水溶液の性質の応用問題として,いくつかの実験を通してそれぞれの水溶液に何が溶けているかを判別する問題があります. このタイプの問題で得点するためには,理科で扱われる水溶液の種類やその性質をそれぞれ正確に理解していなければいけません. ここでは実際の問題を通してこういった問題の解き方を確認しつつ,重要な水溶液の性質を改めて学習していきましょう.
Contents
水溶液の判別問題
実際の入試問題を用いて問題やその解き方を確認していきましょう.
問題

問題の解き方
このような問題ではまず各実験から分かることや,得られた情報のジャンル分けをし,問題用紙に書き込んでいきましょう. まず実験1から分かることを整理していきましょう.
実験1では「AとDが赤色リトマス紙を青色に変化させた」ことが分かります. リトマス紙によって調べられるのは水溶液が酸性・中性・アルカリ性のどの性質をもっているかということです.
赤色リトマス紙を青色に変化させるのはアルカリ性の水溶液です. つまりAとDの水溶液はアルカリ性であるということが分かります.
ここまで情報を得たら,問題用紙の隙間やメモのページに次のように書き込んでおきましょう.
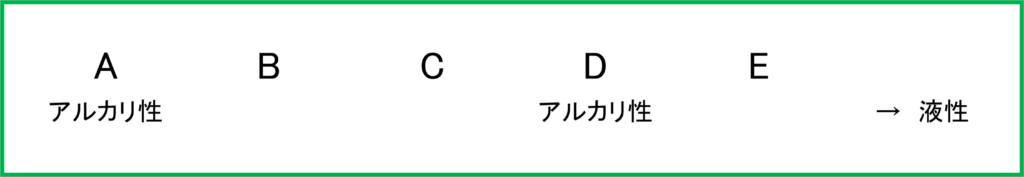
A~Eの性質を下に次々に書き込めるようにこのような一覧を作りましょう. 限られた時間の中でメモをとるうえでは「アルカリ」とだけ書いておくのもいいでしょう.
メモを取る時間を惜しんではいけません. メモを工夫して取っておくことによって自分で情報を整理しやすくなります. 複雑な問題では特に考えるうえで役に立つでしょう.
実験の結果から分かることを書いたら,次の実験を見てみましょう.
実験2では「BとCが青色リトマス紙を赤色に変化させた」ことが分かります.
青色リトマス紙を赤色に変化させるのは酸性の水溶液です. つまり「BとCの水溶液は酸性」であるということが分かります. そしてここで忘れてはいけないのは,「赤色リトマス紙も青色リトマス紙も変化させなかった水溶液Eは中性である」という情報です. これらの情報を次のように書き込んでおきましょう.
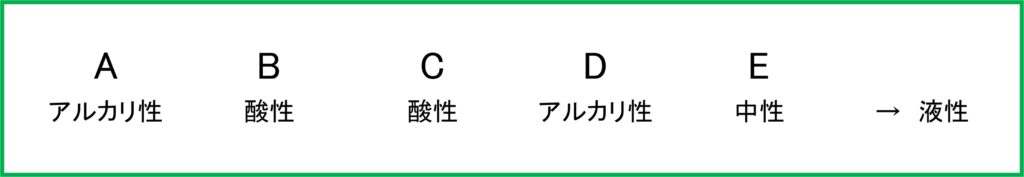
実験1と実験2は同じジャンルの性質に関係するものなので同じ行にまとめてしまいましょう. それでは次の実験を見てみましょう.
次に実験3からは「Bは刺激臭がする」ことが分かります. このことを書き込んでおきましょう.

次に実験4から分かることを整理していきましょう.
まず「Cの水溶液をあたためると気体が出る」ことが分かります.
ここから「Cに溶けている物質は気体」であることが分かります.
液体や固体を水に溶かす時,基本的に温度が上がるとその溶解度は大きくなりますが,気体を水に解かす場合は温度が上がると溶解度が小さくなることが多いです. つまり実験4では水に溶けていた気体が,あたためることによって溶解度が下がり,溶けきれなくなった分が外に出ていっているのです.
そしてさらに「Cに溶けていた気体をAに入れると白く濁った」ことが分かります.
これらをメモしておきましょう.
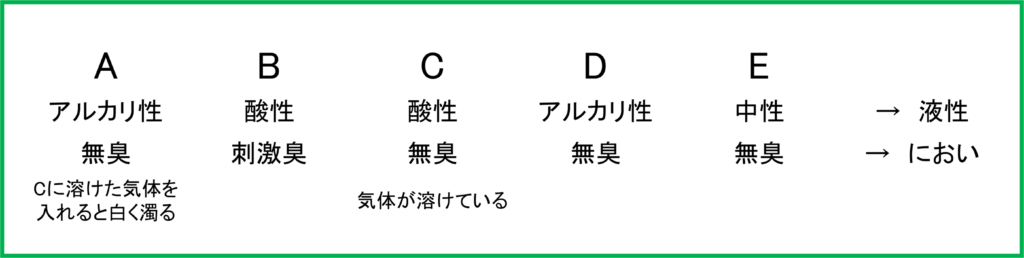
ここまで情報を整理したら,A~Eの水溶液はそれぞれ何が溶けているものであるのかを,①~⑤の選択肢を見ながら特定していきましょう.
まず分かりやすいのは実験4の情報です. 「気体を入れて水溶液が白く濁る」というのは,少なくとも中学受験の範囲では「二酸化炭素を石灰水に入れると白く濁る」ことを指しているにほぼ間違いないでしょう.
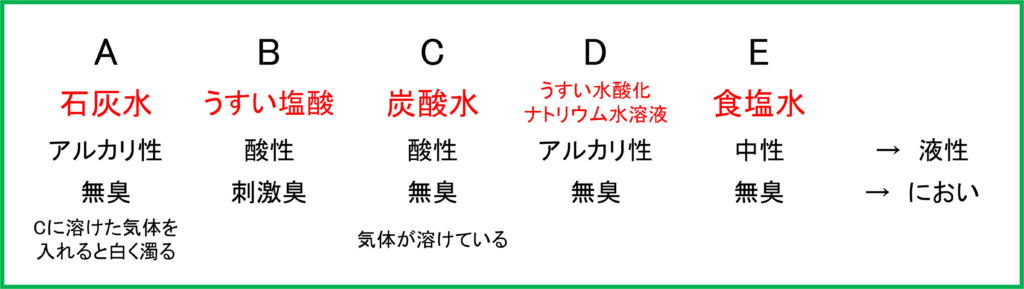
つまり「水溶液Aは石灰水」であり,「水溶液Cは二酸化炭素が溶けた水溶液,つまり炭酸水」であるということになるでしょう.
念のため他の性質とも照らし合わせてみましょう. 石灰水はアルカリ性で無臭の水溶液であり,炭酸水は酸性で無臭の水溶液であるため先ほどメモした特徴とも合致します. これで2つを特定することができました.
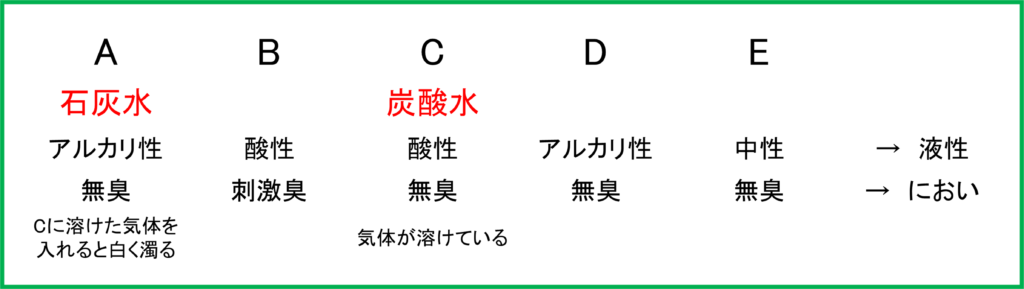
残っている選択肢は「食塩水」,「うすい塩酸」,「うすい水酸化ナトリウム水溶液」なので,これらの液性やにおいの特性と照らし合わせてみましょう. これらの性質は下のようになります.
- 食塩水:中性,無臭
- 塩酸:酸性,刺激臭
- 水酸化ナトリウム水溶液:アルカリ性,無臭
したがってBがうすい塩酸,Dがうすい水酸化ナトリウム水溶液,Eが食塩水であることが分かります.
これらを踏まえて問題を解いていきましょう.

問1と2は上の表より,Cが②,Eが①です.

問3において,BTB液が青色に変化するのはアルカリ性の水溶液であるから,AとDの水溶液があてはまります.

問4は上での解説から,AとDに共通する性質はアルカリ性であるということです.

問5において,各水溶液に何の物質が溶けているかはすでに分かっています.
溶けている物質と,それらがそれぞれ常温で固体か液体か気体かのいずれはそれぞれ下のようになります.
- A:石灰水 → 水酸化カルシウムの水溶液 水酸化カルシウムは固体
- B:うすい塩酸 → 塩化水素の水溶液 塩化水素は気体
- C:炭酸水 → 二酸化炭素の水溶液 二酸化炭素は気体
- D:うすい水酸化ナトリウム水溶液 → 水酸化ナトリウムの水溶液 水酸化ナトリウムは固体
- E:食塩水 → 食塩の水溶液 食塩は固体
よって固体が水に溶けてできたものはA,D,Eです.

問6についてそれぞれの選択肢を見ていきましょう.
- ア:A,すなわち石灰水に鉄を入れても溶けないので間違い.
- イ:B,すなわちうすい塩酸にアルミニウムを入れると水素を出して溶けるので正しい
- ウ:D,すなわちうすい水酸化ナトリウム水溶液にアルミニウムを入れると水素を出して溶けるので正しい
- エ:E,すなわち食塩水に鉄を入れても溶けないので間違い.
つまり選ぶべき選択肢はイ,ウとなります.
金属と水溶液の反応についてはややこしいのでしっかり復習しておきましょう.
問題演習
上のようにして実際の入試問題に挑戦してみましょう.
まずは自分の力で問題を解き,その後下の解答・解説を確認してみましょう.
問題1

問題1-解答
- A:(ウ)
- B:(エ)
- C:(キ)
- D:(ア)
- E:(ク)
- F:(イ)
- G:(カ)
問題1-解説
まず上と同じように各実験から分かることを,ビーカーA~Gのそれぞれについてまとめていくと下のようになります.
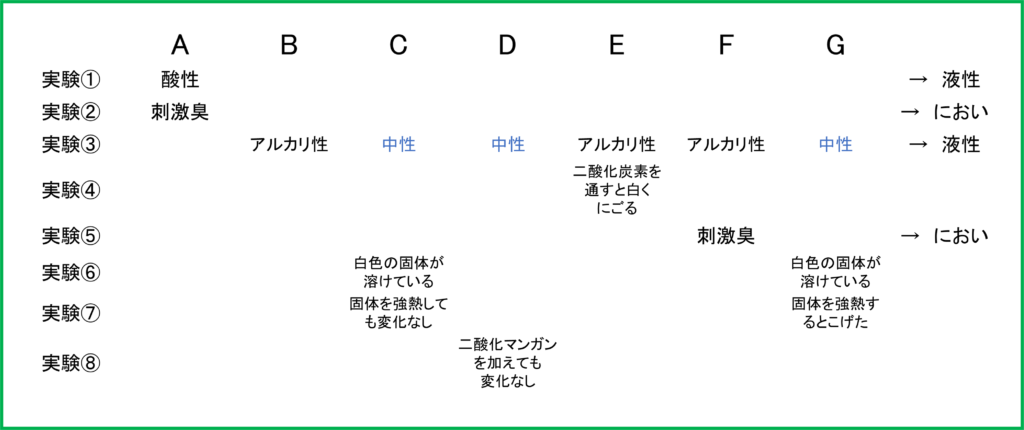
ただし,実験③の中性の部分は実験①で変化しなかったという情報と合わせて確定します.
ここから各水溶液に溶けている物質を特定していきましょう.
酸性・中性・アルカリ性の情報を中心に特定していくのがオススメです.
まずAから特定していきましょう.
「酸性」の水溶液で,選択肢の中から考えられるのは(ウ)のうすい塩酸と(ケ)の炭酸水です.
この中で刺激臭があるのは(ウ)のうすい塩酸の方です. つまりAは「(ウ) うすい塩酸」となります.
そしてA~Gで他に酸性の水溶液がないので「(ケ) 炭酸水」は選択肢から消去してしまいましょう.
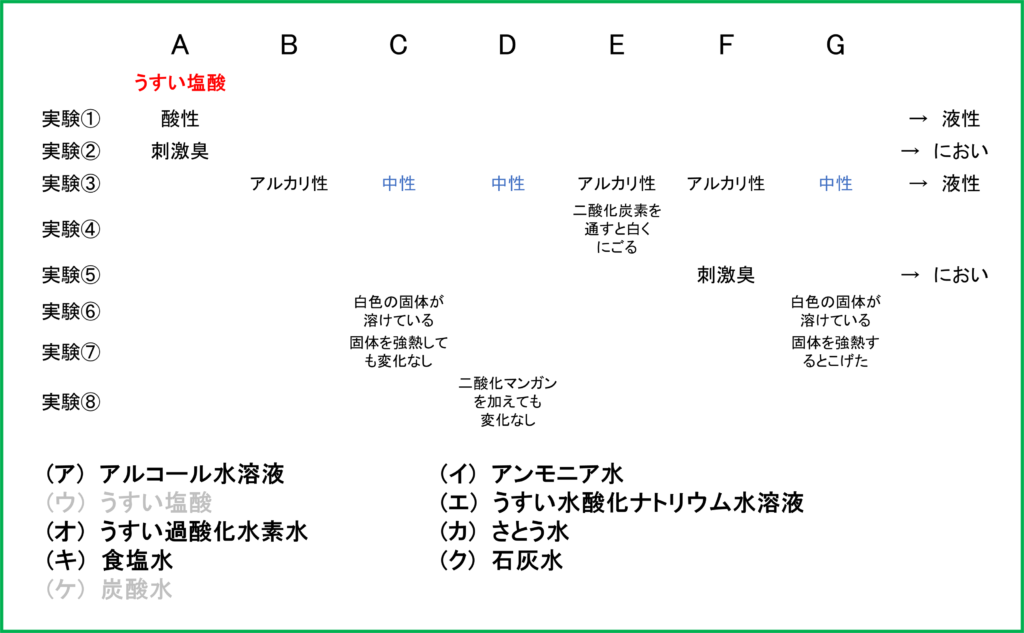
次に「アルカリ性」の水溶液を特定していきましょう.
1番分かりやすいのはEの水溶液でしょう.
「二酸化炭素を通すと白くにごる」とあるので,Eは「(ク) 石灰水」であると分かります.
残りのアルカリ性の水溶液は2つあり,また選択肢の中のアルカリ性の水溶液は「(イ) アンモニア水」と「(エ) うすい水酸化ナトリウム水溶液」です.
この2つにおいてアンモニア水が刺激臭をもつので,Fが「(イ) アンモニア水」でBが「(エ) うすい水酸化ナトリウム水溶液」であることが分かります.
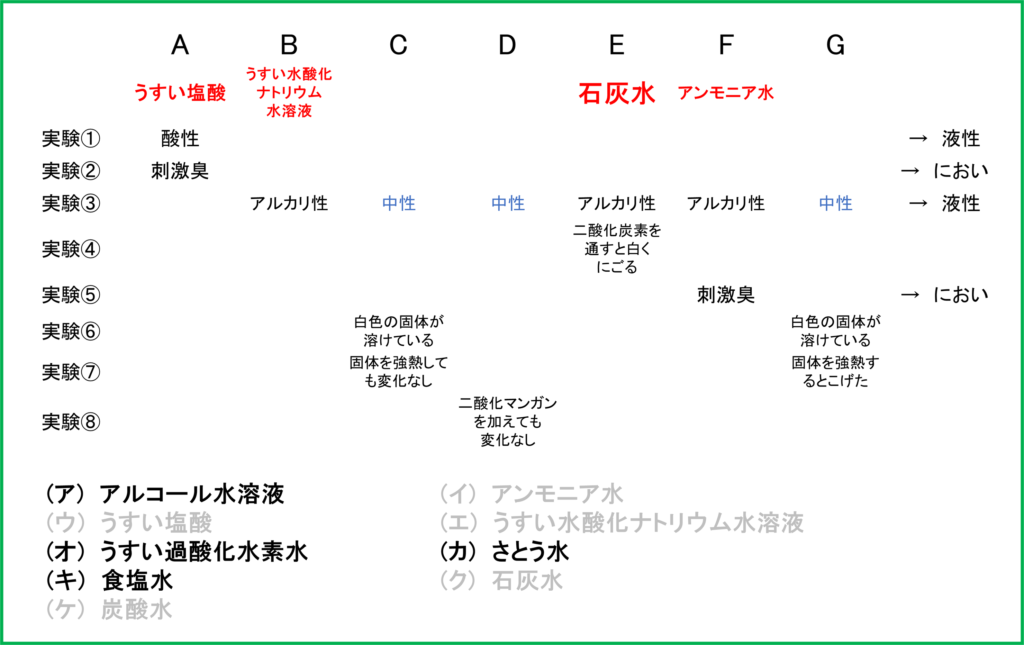
最後に中性の水溶液を特定していきましょう.
主に特徴的なのは「白い固体が溶けている」CとGの水溶液です.
残りの選択肢の中で白い固体が溶けているのは「(カ) さとう水」と「(キ) 食塩水」なのでCとGはそのどちらかになります.
実験⑦の結果から,溶けているのが同じ「白い固体」でも強熱したときに黒くこげるかそうでないかという違いがあります.
強熱したとき,有機物である砂糖は黒くこげますが,無機物である食塩は変化しません. つまりCが「(キ) 食塩水」でGが「(カ) さとう水」となります.
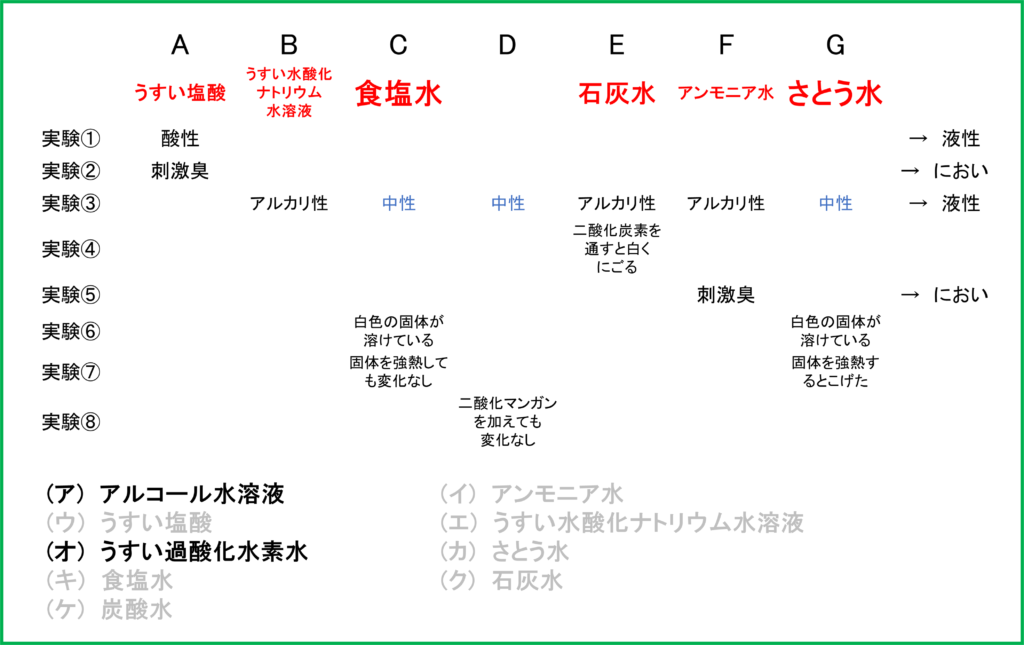
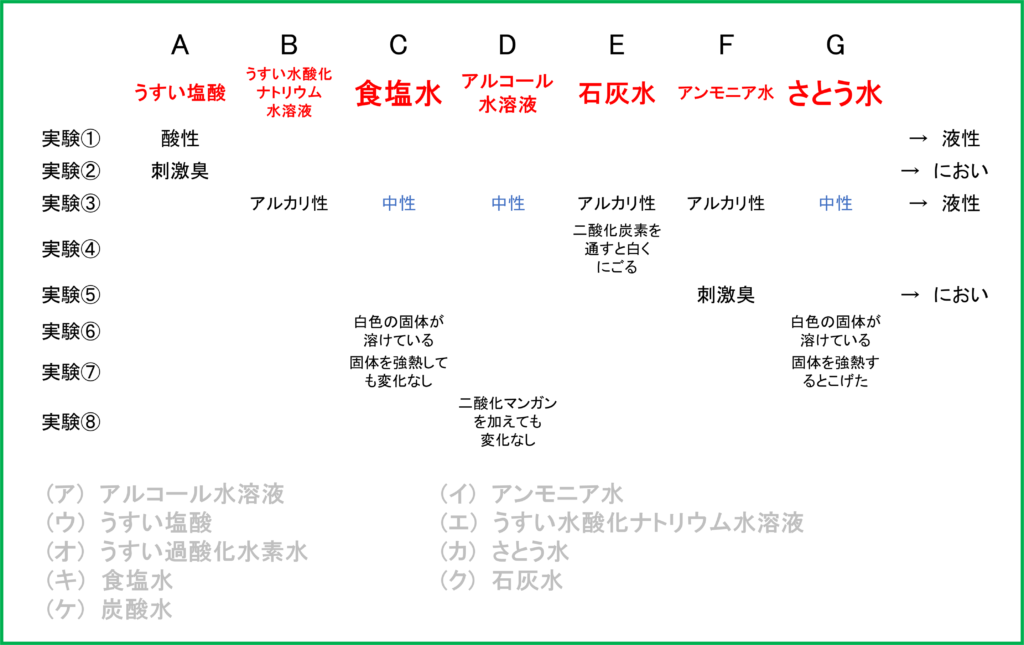
残りはDの水溶液ですが,選択肢から「(ア) アルコール水溶液」か「(オ) うすい過酸化水素水」です.
ここで手掛かりとなるのは実験⑧の結果ですが,「二酸化マンガン」といえば「二酸化マンガンとうすい過酸化水素水を加えると酸素が発生する」という現象が思い出されるのではないでしょうか.
つまりDの水溶液が「(オ) うすい過酸化水素水」であった場合,気体として酸素が発生するはずなのです. しかし実験⑧では変化なしなので,Dの水溶液は残った「(ア) アルコール水溶液」であると分かります.
問題2

問題2-解答
(1)
- 固体:5
- 液体:1
- 気体:3
(2)
- A:2
- B:1
- C:3
- D:7
- E:6
- F:9
- G:5
- H:8
- I:4
(3) 1
問題2-解説
まず上と同じように各実験から分かることを,水溶液 A~Iのそれぞれについてまとめていくと下のようになります.

実験3に関して,加熱してすぐ泡が出てくるものは気体が溶けているものであると考えられます.
問題1と同じように,酸性・中性・アルカリ性の情報を中心に考えていきましょう.
まずは酸性の水溶液です.
選択肢の中で,水に溶かした時に酸性の水溶液となるのは「塩化水素」,「二酸化炭素」,「ホウ酸」です.
まず「刺激臭」のあるAに着目すると,選択肢の中で水溶液が刺激臭を持つものは「塩化水素」を水に溶かした時にできる「塩酸」のみです. よってAは「塩化水素」が溶けていることが分かります.
酸性の水溶液において残りの2つで異なるのは,「気体が溶けているか,固体が溶けているか」です.
「二酸化炭素」が気体で,「ホウ酸」が固体であるので,Fは「ホウ酸」が溶けており,Hは「二酸化炭素」が溶けているということが分かります.

溶けている物質の下の()内は水溶液名が溶けている物質名と異なる場合の名称を示しています.
次にアルカリ性の水溶液を特定していきましょう.
残った選択肢の中で,水に溶かした時にアルカリ性となるのは,「アンモニア」,「水酸化ナトリウム」,「重そう」です.
まず特徴的なBに注目してみましょう.
溶けている物質が気体で,さらに刺激臭があるので,Bは「アンモニア」が溶けたものであるとすぐに分かります.
残りのDとEは「水酸化ナトリウム」,「重そう」のいずれかが溶けていることになります.
注目すべきなのは実験4の結果です.
Eの水溶液では,Aの水溶液,すなわち塩酸と混ぜたときに泡が出ないということに注目しましょう.
「水酸化ナトリウム水溶液」に「塩酸」を混ぜると,中和が起きて「塩化ナトリウム(食塩)」と「水」ができます.
また「重そう水」に「塩酸」を混ぜると,これも中和ができて「塩化ナトリウム(食塩)」と「水」と「二酸化炭素」ができます.
つまりEが「重そう水」であった場合,「塩酸」を混ぜると「二酸化炭素」が発生するので泡が発生するのです.
このことを考えると,Eは「水酸化ナトリウム」が溶けたもの,Dは「重そう」が溶けたものであることが分かります.
さらに中和の結果どちらも「塩化ナトリウム」が生成されるので,実験4の結果から,Gは「食塩」が溶けたものであるということもついでに分かります.
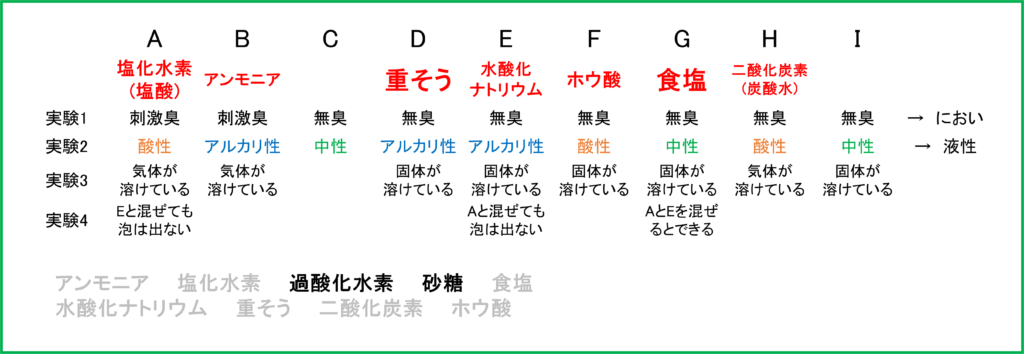
ここで残ったCとIは「過酸化水素」あるいは「砂糖」が溶けたものであるということが分かります.
注目すべきなのは実験3の結果です.
水に溶けてないとき,「過酸化水素」は液体,「砂糖」は固体であるので,Cは「過酸化水素」が溶けたもの,Iは「砂糖」が溶けたものであることが分かります.

これを踏まえて問題を解いていきましょう.

選択肢の物質が水に溶けていない状態はそれぞれ次のようになります.
- アンモニア:気体
- 塩化水素:気体
- 過酸化水素:液体
- 砂糖:固体
- 食塩:固体
- 水酸化ナトリウム:固体
- 重そう:固体
- 二酸化炭素:気体
- ホウ酸:固体
よって溶けていた物質が固体であるものが5個,液体であるものが1個,気体であるものが3個です.

ここは上の結果の通りに番号を選んでいきましょう.
4.5に書いてある解答の通りになります.

問3について,各選択肢を確認していきましょう.
1ではAとD,すなわち「塩酸」と「重そう水」を混ぜると,上に書いた通り中和が起きて「二酸化炭素」が発生するので泡が出ます.
2ではAとF,すなわち「塩酸」と「ホウ酸水」を混ぜても気体は何も発生しません.
3ではEとF,すなわち「水酸化ナトリウム水溶液」と「ホウ酸水」を混ぜると,中和は起きますが気体は何も発生しません. これは難しいので余裕があれば覚えておくくらいでよいでしょう.
4ではEとG,すなわち「水酸化ナトリウム水溶液」と「食塩水」を混ぜても,何も発生しません.
5ではGとI,すなわち「食塩水」と「砂糖水」を混ぜても,何も発生しません.
よって混ぜ合わせたときに泡が発生するのは1のみです.
まとめ
水溶液に溶けている物質を特定する問題では,上で紹介したように酸性・中性・アルカリ性の情報を中心に特定していくと,やりやすいと思います. なので各水溶液が酸性・中性・アルカリ性のいずれであるかは特に重きを置いて覚えておくと良いでしょう.
また上のように実験から得られる結果を整理しながら解くと情報が整理しやすくなるのでぜひこのような問題に出会ったときは試してみてください.
水溶液の性質は様々にあるので繰り返し復習して確実に定着させていきましょう. 物質の写真などを見てより記憶に残りやすくするのもオススメです.


















