Contents
補酵素
酵素の中には、低分子(小さい)の有機物や金属が結合しなければ
活性をもたないものがある。
このような低分子の有機物や金属を補助因子という。
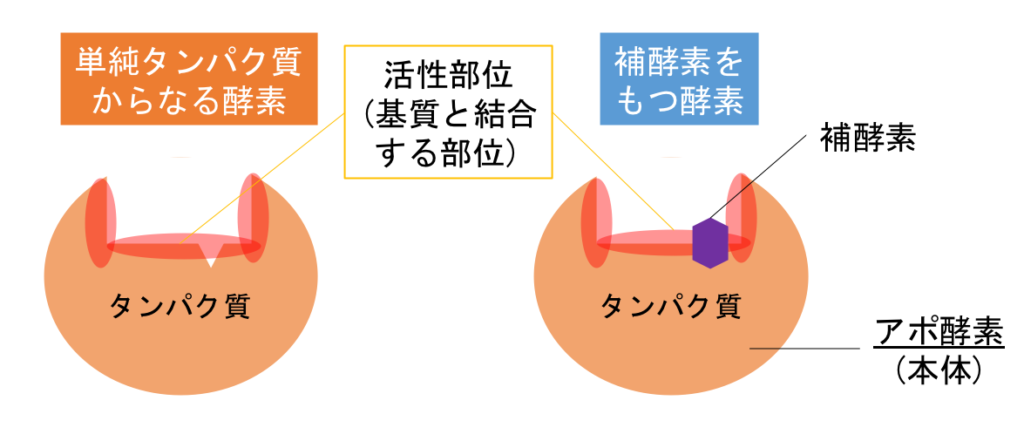
図1 酵素の構造の比較
補酵素
…酵素本体から離れやすい低分子の有機物であり、
透析によってアポ酵素から分離できる。
ビタミンBを成分とするものが多い。
※ビタミンB不足だと代謝異常などが起こる。
例) 脱水素酵素のNAD+ (呼吸)
脱水素酵素のNADP+ (光合成)
脱水素酵素のFAD (呼吸)
※FADは酵素本体から離れにくく、補欠分子族ということがある。

図2 FAD
金属
…酵素に結合したり、酵素活性を高めたりする。
例)カタラーゼのFe、ATPアーゼのMg
透析
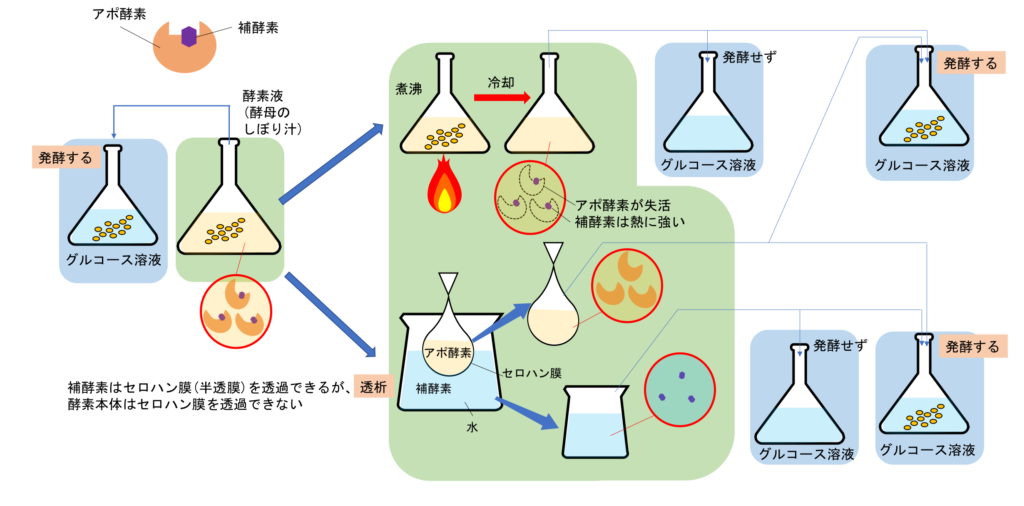
図3 透析 実験概要図
非競争的阻害
アロステリック酵素
酵素の活性部位とは別の場所にアロステリック部位をもつ酵素。
アロステリック部位に立体構造の合う物質が結合すると、
活性部位の立体構造が変化して酵素は失活してしまう。
これをアロステリック効果という。
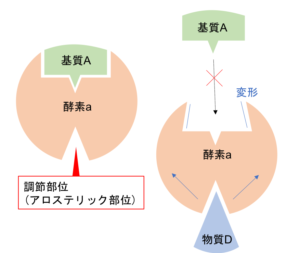
図4 アロステリック部位 構造
フィードバック調節
連続した反応系において、最終産物がはじめの酵素aの
アロステリック部位に結合すると反応系全体が抑制される。
このように、最終産物がはじめの段階に戻って
反応を調節する仕組みをフィードバック調節という。
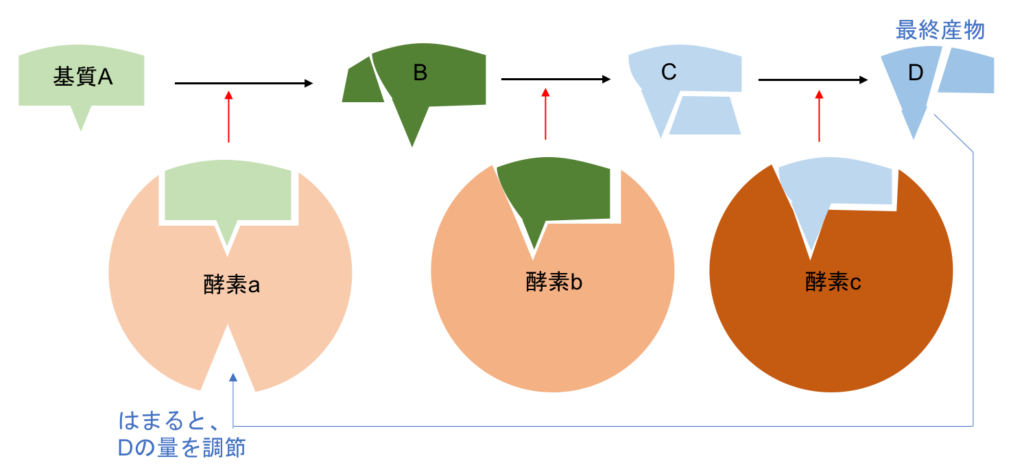
図5 フィードバック調節 構造
競争的阻害
基質と立体構造のよく似た物質(阻害物質)が、
酵素の活性部位に結合して反応を阻害する。
例)マロン酸によるコハク酸脱水素酵素の阻害
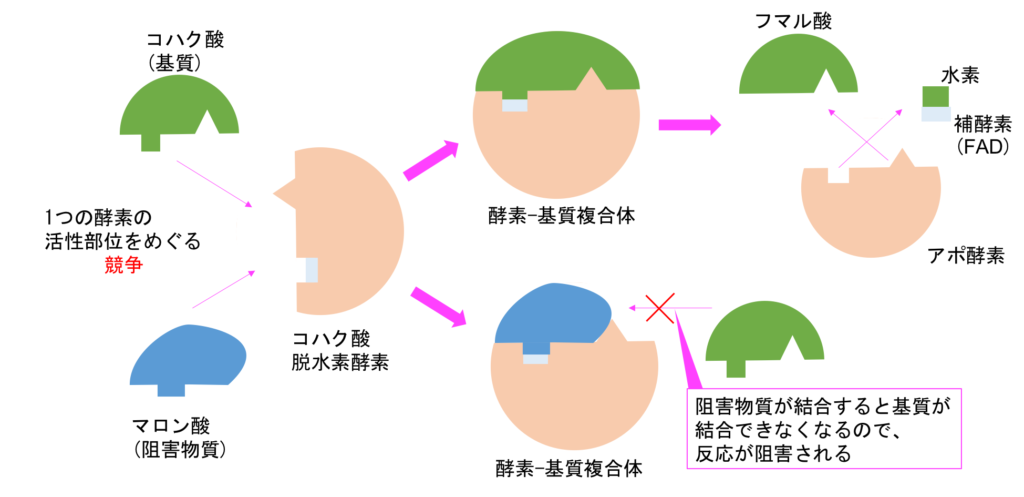
図6 マロン酸によるコハク酸脱水素酵素の阻害 構造
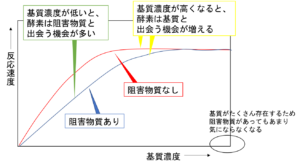
図7 基質濃度と反応速度の関係
例題
酵素反応と阻害物質
【問題】下の図aは、一定の酵素濃度のもとで基質濃度と酵素反応速度との関係を示している。以下の問いに答えよ。
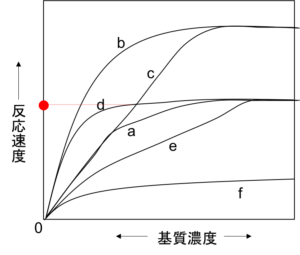
図a
(問1)基質濃度が高くなると反応速度は一定になるが、このときの反応速度を何というか。
(問2)問1のとき、酵素と基質はどのような状態になっていると考えられるか、簡単に説明せよ。
(問3)酵素濃度を2倍にした場合、反応速度はb~fのどれになるか。
(問4)反応液に、基質と化学構造が似ており、活性部位と結合する物質を加えた場合、反応速度はb~fのどれになるか。
(問5)反応液に、酵素の活性部位とは異なる場所に結合し、酵素活性を低下させる物質を加えた場合、反応速度はb~fのどれになるか。
【解答】
- (問1)(・の点のこと)最大反応速度
- (問2)すべての酵素が基質と結合して、酵素-基質複合体となっている状態。
- (問3)(=反応速度2倍) b
- (問4)基質と化学構造が似ており、活性部位と結合する物質(→競合的阻害) e
- (問5)酵素の活性部位とは異なる場所(=アロステリック部位)に結合〜 f
知識の確認
最後に簡単な問題を出したいと思います。ぜひ知識の確認に役立ててみてください。
【問題】
・問1:アロスティック部位に立体構造の合う物質が結合すると、酵素が失活してしまう。この効果を何というか
・問2:最終産物がはじめの段階に戻って反応を調節する仕組みを何というか
【模範解答】
・問1:アロスティック効果
・問2:フィードバック調節
最後に
登録6000人以上!
本サイト、中学受験ナビの監修も務めている『開成番長』こと繁田和貴が執筆する完全無料のメールマガジンでは、主に中学受験生のお子さんをお持ちの方へ向けた様々なお役立ち情報を配信中!
さらに今なら登録者にはもれなく「開成番長・繁田の両親が語る繁田の中学受験PDF」をプレゼント!
登録及び登録解除も簡単ですので、お気軽にご登録ください。











